Original: http://www.tulane.edu/~wiser/malaria/cmb.html
Представники роду Plasmodium є еукаріотичні мікроорганізми. Таким чином, клітинна і молекулярна біологія Plasmodium буде схожа на інших еукаріотів. Унікальною особливістю малярійного паразита є його внутрішньоклітинний спосіб життя. Через його внутрішньоклітинної локалізації паразита має близькі стосунки з його кліткою-хазяїном, яка може бути описана на клітинному і молекулярному рівнях. Зокрема, паразит повинен проникати в клітку-господаря, і як тільки всередині, він змінює клітини-господаря. буде обговорюватися молекулярної і клітинної біології господар-паразит взаємодій, що беруть участь в цих двох процесах.
Зміст:
– Вторгнення хост еритроцитів
– Первісний зв’язок і MSP-1
– Переорієнтація і секреторні органели
– Розподільна Формування і Microneme Білки
– Вхід паразита
– Ковзаючи моторику і Glidosome
– Резюме
– Хост Модифікація еритроцитів
– Knobs і Cytoadherence
– Ендотеліальні Рецептори клітин
– антигенна мінливість
– резюме
– посилання
– зв’язки
Введення
Вторгнення в клітину господаря
Паразити малярії є членами Apicomplexa. Apicomplexa характеризуються набором органел, знайдених в деяких стадіях життєвого циклу паразита. Ці органели, відомі як апікальних органел через їх локалізації в одному кінці паразита, беруть участь у взаємодії між паразитом і господарем. Зокрема, апікальні органели беруть участь в процесі вторгнення клітини-господаря. У разі Plasmodium, три різних інвазивні форми були ідентифіковані: спорозоїтів, мерозоитов і ookinete (див Plasmodium Життєвий цикл). Далі мова піде про клітинної біології мерозоїтів і еритроцитарної вторгнення. Посилання на інші Apicomplexa і Plasmodium спорозоїтів будуть зроблені, щоб проілюструвати загальні риси.
Мерозоитов вторгнення Мерозоїти швидко (приблизно 20 секунд) і, зокрема входять еритроцитах. Ця специфічність виявляється як для еритроцитів як пріоритетний тип клітини-господаря, і для конкретного виду господаря, таким чином, що передбачає взаємодію рецептор-ліганд. Erythrocyte вторгнення являє собою складний процес, який лише частково розуміти на молекулярному та клітинному рівнях. Проте, значний прогрес був досягнутий у визначенні багатьох паразита і господаря білків, які є важливими для процесу вторгнення.
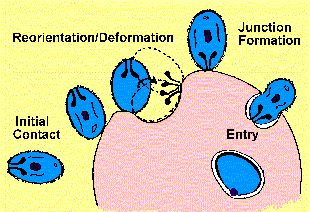
Чотири окремих технологічних операцій (Gratzer and Dluzewski 1993) в процесі вторгнення можуть бути визнані (малюнок):
початкові обов’язкові мерозоїтів
переорієнтації та деформації еритроцитів
формування переходу
вхід паразита
Мерозоитов поверхневих білків і господар-паразит взаємодій
Початкове взаємодія між мерозоїтів і еритроцитах, ймовірно, випадкове зіткнення і, імовірно, включає в себе оборотні взаємодії білків на поверхні мерозоїтів і приймаючої еритроцита. Кілька мерозоитов поверхневих білків були описані. Найбільш добре охарактеризованих є мерозоитов поверхневий білок-1 (ПНС-1). Непрямі докази причетності MSP-1 в еритроцитах вторгнення включає в себе рівномірний розподіл його по поверхні мерозоїтів і спостереження, що антитіла проти MSP-1 пригнічувати інвазію (Holder 1994). Крім того, MSP-1ДЕЛАЕТ зв’язуються з 3-й зоні (Goel 2003). Проте, роль MSP-1 в вторгнення не було остаточно продемонстровано. Точно так же, білок ціркумспорозоітного (СКП), можливо, грає певну роль в орієнтації спорозоїти гепатоцитів шляхом взаємодії з гепарин сульфат протеоглікани (Sinnis and Sim 1997).
Ще один цікавий аспект МСП-1 є протеолітичний процесинг, збігається з мерозоитов дозріванням і інвазії (Cooper 1993). Первинна обробка відбувається в момент дозрівання merozite і призводить до утворення декількох поліпептидів, скріплених в Нековалентні комплексу. Вторинна обробка відбувається збігаються з мерозоитов вторгненням на ділянці поблизу С-кінця. Нековалентні комплекс MSP-1 поліпептидних фрагментів проливається від поверхні мерозоїтів наступні протеолиз і тільки невеликий С-кінцевий фрагмент переноситься в еритроцитах. Ця втрата MSP-1 комплексу може корелювати з втратою “розмитих” пальто під час мерозоїти вторгнення. С-кінцевий фрагмент приєднаний до поверхні мерозоїтів з допомогою якоря GPI anchor і складається з двох EGF-подібних модулів. EGF-подібних модулів виявлені в різних білків і, як правило, беруть участь в білок-білкових взаємодій. Одним з можливих варіантів є те, що вторинні протеолітичні функції обробки, щоб виставити EGF-подібні модулі, які підсилюють взаємодію між мерозоїтів і еритроцита. Важливість ССП-1 і його переробки випливають з наступних спостережень:
– Вакцинація з EGF-подібних модулів може захистити від малярії, і
– інгібування блоків обробки протеолітичний мерозоїти вторгнення.
Точна роль (и), які МСП-1 і його обробка грають в процесі його інвазії мерозоитов не відомі. Інші білки мерозоитов поверхні також беруть участь в Інтерактивного з мерозоїти з еритроцита (Cowman 2012).
Переорієнтація і секреторні органели
верхівковий органел
Plasmodium Мерозоїти
Органел Форма Розмір (нм)
Microneme еліпсоїдальної 40 х 100
Rhoptry сльозинки 300 х 600
Щільні Гранула сферична 120-140
Після зв’язування з еритроцита, паразит переорієнтує себе так, що «верхівковий кінець» паразита зіставляється мембрани еритроцита. Це мерозоитов переорієнтація також збігається з транзиторною деформації еритроцитів. Апікальний мембранний антиген-1 (АМА-1) бере участь у цій переорієнтацією (Mitchell 2004). АМА-1 являє собою трансмембранний білок, локалізований на апікальній кінці мерозоїтів і зв’язується еритроцитами. Антитіла проти АМА-1 не INTERFER з початковим контактом між мерозоїтів і еритроцита, таким чином, припускаючи, що АМА-1 не бере участі в мерозоїти прикріпленого. Але антитіла проти АМА-1 запобігти переорієнтацію мерозоїти і тим самим блокують мерозоитов вторгнення.
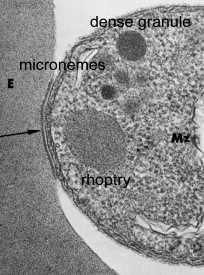
Спеціалізований секреторні органели розташовані на апикальном кінці інвазійних стадій апікомплексні паразитів. Три морфологічно різних вершинні органели виявлені за допомогою електронної мікроскопії: micronemes, rhoptries і щільних гранул (таблиця). Щільні гранули не завжди включаються з верхівкових органел і, ймовірно, являють собою гетерогенну популяцію секреторних везикул.
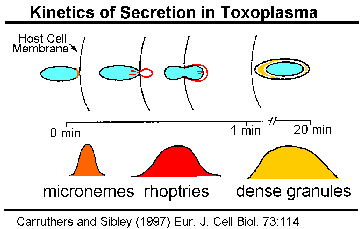
Кінетика зміст SecretionThe верхівкового органел викидаються, як паразит проникає, тим самим припускаючи, що ці органели грають певну роль в інвазії. Експерименти в токсоплазма показують, що micronemes викидаються першого і відбуваються з початковим контактом між паразитом і господарем (Carruthers and Sibley 1997). Збільшення цитоплазматичної концентрації кальцію пов’язано з microneme розрядом і, ймовірно, включає в себе сигнальний шлях за участю фосфоліпазу С, inositoltriphosphate і залежні протеїнкінази кальцію (Sharma and Chitnis 2013).
У rhoptries виписують відразу ж після того, як micronemes і вивільнення їх вмісту корелюють з утворенням паразітофорной вакуолі.
Щільні вмісту гранул вивільняються після того, як паразит завершив свій запис, і, отже, як правило, беруть участь в модифікації клітини-господаря. Проте, субтілізін протеаз, які беруть участь в вторинної протеолітичного процесингу MSP-1 (вище), також були локалізовані в Plasmodium щільних гранул (Blackman 1998, Barale 1999). Якщо обробка MSP-1 каталізується цими протеаз, то, по крайней мере, деякі щільні гранули повинні відводитися в момент вторгнення.
Специфічні взаємодії і Junction Формування
Слідом за мерозоитов переорієнтацію і microneme розрядити розподільну форми між паразитом і клітиною-господарем. Мабуть, microneme білки мають важливе значення для формування з’єднання. Білки локалізується в micromenes включають:
EBA-175, 175 кДа ‘еритроцита зв’язування антигену’ з P. малярійного
DBP, Даффі-зв’язуючий білок з P. триденної і П. knowlesi
SSP2, Plasmodium спорозоїтів поверхневий білок-2. Також відомий як TRAP (тромбоспондину пов’язаних з клейкого білка).
Білки з гомологичной SSP2 / TRAP від токсоплазми (MIC2), Егтепа (Etp100) і Cryptosporidium
ЧТПЗ, circumsporozoite- і TRAP пов’язаних білка Plasmodium знаходиться в стадії ookinete
Рецептор / ліганд
Види Хост Рецептор мерозоитов Ліганд
П. малярійного глікофорину (сіалова кислоти) EBA-175
П. триденної,
П. knowlesi Даффі антиген DBP
Особливо слід відзначити EBA-175 і ДАТ, які визнають залишки сіалова кислоти глікофорину і антигену Duffy, відповідно (таблиця). Іншими словами, ці паразитні білки, ймовірно, беруть участь у взаємодії з рецептором лиганда з білками, що виставляються на поверхні еритроцита. Зрив результатів EBA-175 генів в паразита переходу від кислотно-залежного шляху сиаловой до кислотно-незалежного шляху сиаловой (Reed 2000), вказуючи, що є деяка надмірність щодо взаємодії рецептор-ліганд.
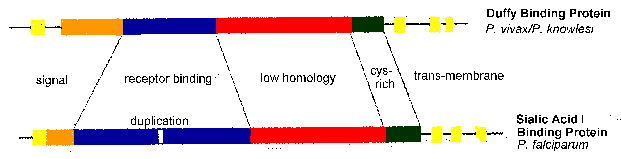
Порівняння послідовностей EBA-175 і ДАТ виявити зберігаються структурні особливості. До них відносяться трансмембранні домени і рецептор-зв’язуючі домени (рис, модифіковані з Adams 1992). Активність рецептора зв’язування був зіставлений з доменом, в якому цистеїн і ароматичні амінокислотні залишки зберігається між видами (синя область на малюнку). Цей уявний зв’язує домен дублюється в EBA-175. Топографія трансмембранного домену узгоджується з лігандами паразитів, які є інтегральні мембранні білки з доменом зв’язування рецептора, виставленому на поверхні мерозоїтів наступні microneme розряду.
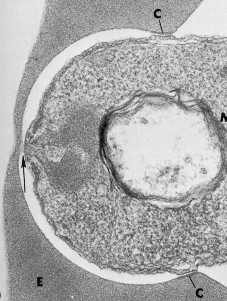
Розподільна Формування Microneme реліз
Стрілка позначає електрон щільне з’єднання між мерозоїтів і еритроцита. Мікрофотографія з Айкава і ін (1978) J. Cell Biol. 77:72.
EBA-175 і ДАТ є частиною сімейства adhesins, знайдених в малярійних паразитів зазвичай називають EBL для eyrthrocyte-зв’язуючим подібне. Інша сімейство адгезінов, що беруть участь в зв’язуванні мерозоитов до erthrocytes є ретикулоцитів-зв’язуючим як гомологів (Rh). Ці різні адгезінов зв’язуються з різними рецепторами на еритроцитах і забезпечити надмірність в здатності мерозоїти з утворенням стику з еритроцита (Tham 2012). Рецептор basigin може мати важливе значення для вторгнення в P. малярійного (Crosnier 2011).
Інші білки microneme в ‘TRAP’ сім’ї також залучені в руховий апарат і / або інвазії клітин на стадії спорозоїтів і інших Apicomplexa (Tomley and Soldati 2001). Всі ці білки (EBL, Rh, TRAP сімей) домени, які, ймовірно, залучені в міжклітинної адгезії, а також трансмембранний домени на їх C-кінцях. Microneme реліз піддасть адгезійні домени, які потім зв’язуються з рецепторами на клітині-хазяїні і, таким чином, утворюють з’єднання між інвазивної формою (наприклад, мерозоїти) і клітини-господаря (рис).
Іншим елементом цього злиття включає в себе білки, знайдені в шийці rhopthry, зокрема Ron2. Ron2 є звільнення від rhoptry і вставляється в мембрану еритроцита. Ron2 потім зв’язується з АМА-1, який локалізований на поверхні мерозоїтів (Tonkin 2011). Ron2 / АМА-1 комплекс потім також сприяє цьому щільного контакту, утвореного між мерозоїтів і еритроцита. Фосфорилювання AMA -1 може також брати участь у записі паразита (Leykauf 2010).
У підсумку:
електрон-щільні форми з’єднання між верхівкової кінця мерозоїти і господар мембрани еритроцита відразу після переорієнтацією
формування щільні контакти і випуск microneme відбуваються приблизно в той же час
білки локалізовані в micronemes зв’язуються з рецепторами на поверхні еритроцита
Білки в шийці rhoptry вставляються в хост-мембрану і зв’язуються з АМА-1 на merozite поверхні з утворенням щільного контакту
Ці спостереження вказують на те, що вузол являє собою міцний зв’язок між еритроцита і мерозоїти, який опосередковується взаємодією рецептор-ліганд. формування Junction може бути ініційовано microneme розрядом з подальшим виділенням rhoptry шиї білків, які виставляє домени рецептор-зв’язуючих паразита лігандів. Цей механізм ініціювання щільної взаємодії господар-паразит схожий на інших інвазивних стадіях апікомплексні паразитів.
Вхід паразита
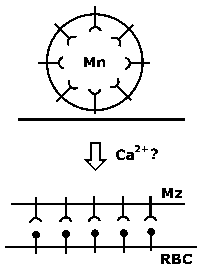
Апікомплексні паразити активно вторгатися в клітини-господарі і запис не через поглинання або фагоцитоз клітиною-господарем. Це особливо очевидно в разі еритроцита, який відчуває нестачу здатності фагоцитів. Крім того, еритроцит мембрана має 2-мірну підмембранну цитоскелету виключає ендоцитоз. Таким чином, імпульс для формування паразітофорной вакуолі повинна виходити від паразита. Кілька подій сталося під час запису паразита в тому числі: 1) зриву подмембранное цитоскелета еритроцита, 2) формування паразітофорной вакуолі і 3) і пролиття мерозоитов поверхневих білків. Паразит запис приводиться в рух за допомогою ACTO-міозину моторного комплексу під назвою glidosome.
Еритроцитарна мембранні білки перерозподіляються в момент формування з’єднання таким чином, що площа контакту вільний від білків мембран еритроцитів. Серін-протеази мерозоитов який розщеплює еритроцит смуга 3 була описана (Braun-Breton 1993). Через ключової ролі групи 3 грає в гомеостазу з подмембранное скелета, його деградація може привести до локального порушення цитоскелету. Реорганізація подмембранное цитоскелету і ліпідного архітектури, ймовірно, супроводжує мерозоитов вторгнення (Zuccala 2011).
мерозоитов
Мікрофотографія з Айкава і ін (1978) J. Cell Biol. 77:72
Зароджується паразітофорной вакуольна мембрана (ПЗМ) утворюється в зоні стику. Ця мембрана впячивание, ймовірно, походить від як господар мембрани і паразитарних компонентів і розширюється, як паразит проникає в еритроцит. Зв’язки між rhoptries і зароджується PVM іноді спостерігаються (рис, стрілка). Крім того, вміст rhoptries часто пластинчасті (тобто багатошарові) мембрани і деякі rhoptry білки локалізовані в PVM після вторгнення, припускаючи, що rhoptries також функціонують у формуванні PVM (Sam-Yellowe 1996).
Ookinetes відсутність rhoptries і не утворюють паразітофорной вакуоль в межах комар епітеліальних клітин середньої кишки. У ookinetes швидко проходять через епітеліальні клітини і викликають значної шкоди, як вони спрямовуються до базальної пластинки (Han 2000, Ziegler 2000). Точно так же, спорозоїти можуть входити і виходити з гепатоцитів без проходження exoerythrocytic Шизогонія. Ці паразити, що не зазнають Шизогонія вільні в приймаючої цитоплазмі, в той час як ті, які проходять Шизогонія укладені всередині PVM (Mota 2001). Ці спостереження вказують на те, що ПВМ необхідний для внутрішньоклітинного розвитку і не є необхідним для процесу вторгнення клітини-господаря. Як формується починається паразітофорной вакуоль, з’єднання (позначений с х в малюнку) між паразитом і господарем стає кільцеподібне і паразит з’являється рухатися через цей кільцевої зазор, як надходить в розширюється паразітофорной вакуоль. Замість того, щоб це переміщення спай тягне від передньої частини паразита до задньої частини, що призводить до руху вперед паразита в клітку-господаря.
Як надходить паразит, MSP-1 багато з поверхневих білків мерозоїтів опадає. Цей процес линьки опосередковано специфічними протеазами і являє собою упорядкований процес (Boyle 2014).
Glideosome
Інвазивні форми апікомплексні паразитів часто рухомі форми, які сканують по субстрату за типом перистальтики називають “ковзним моторики ‘. Ковзаючи моторику, як вторгнення, також включає в себе випуск micronemal адгезінов, прикріплення до субстрату, і закупорювання адгезінов на задньому кінці zoite. Одне з відмінностей між змінним моторики і вторгненням в тому, що micronemes повинен постійно випущений як організм рухається. Таким чином, ковзаючи моторику не тягне за цей відносно невеликий рухомий перехід, але безперервне утворення нових з’єднань між zoite і субстрату. Крім того, адгезінов отщепляют від поверхні zoite як спайки досягають апостеріорне zoite і слід адгезійних молекул залишають за рухомим zoite на субстраті. Механізм рухливості і інвазії дуже схожі, і, таким чином, під час навали паразит буквально повзає в клітку-господаря через рухомий вузол. Крім того, деякі apicomplexans використовують цей тип моторики, щоб вирватися з клітин і можуть перетинати біологічні бар’єри, входу і виходу з клітини.
glidosome.
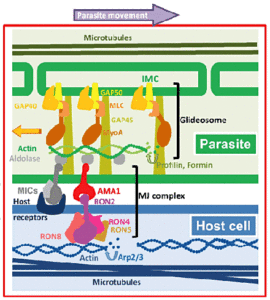
Cytochalasins інгібують запис мерозоитов, але не прихильність, тим самим припускаючи, що сила, необхідна для вторгнення паразита і ковзаючи моторики заснований на актин-міозин елементів цитоскелету. Здатність міозину, білок двигуна, щоб генерувати силу, добре відомо (наприклад., Скорочення м’язів). Міозину унікальний для Apicomplexa був ідентифікований і закріплена у внутрішній комплекс мембрани (IMC). IMC відноситься до подвійною мембраною, що лежить під мембраною плазми на інвазивні стадіях апікомплексні паразитів. Цей IMC додатково підтримується суб-плівкова микротрубочек, які керують довжиною паразита. СИН, пов’язаний міозин взаємодіє з актином в складі glidesome. Різні адгезінов (тобто EBL, Rh, TRAP і АМА-1), що утворюють комплекс рухомий розподільну (MJ) потім пов’язані з glidesome (малюнок).
Модель рухається з’єднання комплексу і glidesome водіння ковзають моторику від Besteiro (2011).
Члени сім’ї пасткою і інших адгезінов мають зберігається цитоплазматический домен. Цей цитоплазматический домен пов’язаний з короткими актінових филаментов за допомогою альдолази. Ниток актину і міозину орієнтовані в просторі між внутрішнім комплексом мембрани і плазматичноїмембрани таким чином, що міозин розганяє актинові філаменти у напрямку до заднього zoite. Міозину закріплений в IMC і не рухається. Таким чином, трансмембранний адгезінов втягуються через рідино ліпідний бішар мембрани плазми через їх асоціації з Актинові філаментів. Таким чином, комплекс адгезінов і Актинові філаментів транспортується в напрямку задньої частини клітини. Так як адгезінов або у вигляді комплексу з рецепторами на клітині-хазяїні, і прикріплюється до цитоскелету клітини-господаря, або пов’язаний з субстрату, чистий результат є поступальний рух паразита (малюнок). Коли адгезінов досягають заднього кінця паразита вони proteolyitcally розщеплюється і пролив від zoite поверхні.
У разі вторгнення клітин клітинної мембрани ПВМ і хост буде необхідно герметизовані таким чином, що ПВМ ціла і оточуючих паразита і господаря плазматическую мембрану також недоторканим. Механізми, що беруть участь в цій останній стадії вторгнення не відомі.
резюме
Мерозоитов вторгнення являє собою складний і упорядкований процес. Попередня модель мерозоїти вторгнення включає в себе:
Початкове мерозоитов зв’язування включає оборотні взаємодії між поверхневими білками мерозоитов і господаря erythrocyte.The точні ролі MSP1 і інших поверхневих білків мерозоїтів, не відомі.
Переорієнтація невідомим призводить механізм в апикальном кінці мерозоїтів будучи примикає до мембрани еритроцита.
Розрядка micronemes збігається з утворенням щільного контакту між хостом і паразитами. Щільні контакти опосередковується взаємодією рецептор-ліганд між поверхневими білками еритроцитарних і паразитарних Інтегральні мембранні білки, які буде розкрито microneme розрядом.
Локалізовані очищення еритроцита подмембранное цитоскелету і формування зароджується паразітофорной вакуолі. формування PVM корелює з розрядом з rhoptries.
Рух мерозоїти через кільцеподібну щільного контакту, утвореного рецептор / ліганд. Сила породжується миозинових моторів, пов’язаний з трансмембранної паразит ліганди рухається уздовж ниток актину в паразита.
Закриття PVM і мембрани еритроцита.
Багато білки, які беруть участь в процесі вторгнення були ідентифіковані. Це буде також включати в себе події між різними етапами вторгнення (Santos and Soldati-Favre 2011) сигналізації. Проте, багато що ще належить дізнатися про клітинному і молекулярної біології мерозоїтів вторгнення. Краще розуміння складного процесу вторгнення паразита може привести до розробки нових терапевтичних підходів до малярії та інших захворювань, викликаних Apicomplexans.
HOST ЕРИТРОЦИТІВ МОДИФІКАЦІЯ
Опинившись всередині еритроцита, паразит проходить фазу трофічної з подальшим репликативной фази. Протягом цього періоду intraerythrocytic, паразит змінює хост, щоб зробити його більш підходяще місце проживання. Наприклад, еритроцит мембрана стає більш проникною для малих метаболітів молекулярного ваги, мабуть, відображають потреби активно зростаючого паразита (див Uptake and Permeability).
Інша модифікація клітини-господаря стосується cytoadherence П. тропічної малярії інфікованих еритроцитів ендотеліальних клітин і в результаті секвестр зрілих паразитів в капілярах і після венул. Цей секвестр ймовірно призводить до мікроциркуляторних змін і метаболічних порушень, які можуть бути відповідальні за багато з проявів важкої триденної малярії (див pathogenesis). Cytoadherence ендотеліальних клітин дає принаймні, дві переваги для паразита: 1) мікроаерофільна середовища, яка краще підходить для паразита обміну речовин, і 2) уникнення селезінки і подальшого руйнування.
Knobs і Cytoadherence
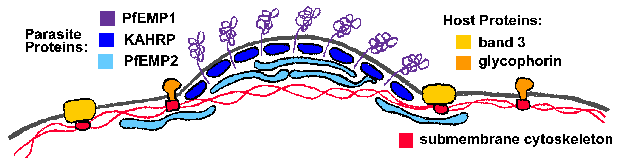
Основним структурним зміною приймаючої еритроцита є електронно-щільні виступи, або «ручки», на еритроцитарної мембрані P. фальціпарум-інфікованих клітин. Регулятори викликаються паразитами і кілька паразитів білки пов’язані з ручками (Deitsch and Wellems 1996). Два білка, які можуть брати участь у формуванні ручки або впливають на господаря еритроцита подмембранное цитоскелету і побічно індукують утворення ручки є ручки-асоційованої гистидин багатих білком (KAHRP) і еритроцитах мембранний білок-2 (PfEMP2), званий також Mesa. Ні KAHRP ні PfEMP2 виставлені на зовнішній поверхні еритроцита, але локалізовані на цитоплазматичної поверхні мембрани господаря (малюнок). Їх точні ролі в формуванні ручки не відомі, але можуть включати в себе реорганізацію підмембранна цитоскелета.
Структура ручки
Регулятори вважають, відіграють певну роль в секвестрації заражених еритроцитів, так як вони є точками контакту між зараженим еритроцита і судинних ендотеліальних клітин і видів паразитів, які висловлюють ручки демонструють найвищі рівні секвестру. Крім того, руйнування KAHRP призводить до втрати ручок і здатності cytoadhere в проточних умовах (Crabb 1997). Поліморфний білок, званий PfEMP1, також була локалізована на ручки і виставлено на поверхні господаря еритроцита. Транслокацию PfEMP1 на поверхні еритроцита залежить частково від другої мембрани еритроцитів, пов’язаного білка під назвою PfEMP3 (Waterkeyn 2000). PfEMP1 ймовірно функціонує в якості ліганда, який зв’язується з рецепторами на хост ендотеліальних клітинах. Інші запропоновані cytoadherence ligands включають модифікований зонний-3, названий pfalhesin (Sherman 1995), sequestrin, rifins і clag9 (Craig and Scherf 2001).
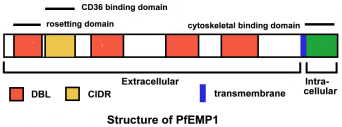
PfEMP1 є членом гена сімейства вар (Hviid 2015). Кожен паразит має оцінені гени 40-60 Var, які демонструють високу ступінь мінливості, але мають такий же загальну структуру (малюнок). PfEMP1 має великий позаклітинний N-кінцевий домен, трансмембранний ділянку і С-кінцевий внутрішньоклітинного домен. C-кінцевий області зберігається між членами сім’ї вар і вважається, що якір PfEMP1 до еритроцитарної подмембранное цитоскелету. Зокрема, цей кислотний С-кінцевий домен може взаємодіяти з базової KAHRP ручки (Waller 1999), а також спектрин і актину (Oh 2000).
Позаклітинний домен характеризується 1-5 копій Даффі зв’язування, як (DBL) доменів. Ці домени DBL аналогічні області зв’язування рецептора лігандів, що беруть участь в мерозоїтів інвазії (описано вище). ДВМ домени демонструють законсервовані відстань між цистеїну і гідрофобних залишків, але в іншому проявляють мало гомології. Філогенетичний аналіз вказує на те, що існує п’ять різних класів (позначених як, б, г, д, е) областей DBL (Hviid 2015). Перший ДВМ завжди той же самий тип (позначений а), і це супроводжується междоменной області багатих цистеїном (CIDR). Мінлива кількість DBL в різних замовлень складають іншу частину позаклітинного домену PfEMP-1.
Під час кожного митотического циклу гени вар пройти процес рекомбінації призводить до безперервної генерації додаткових варіантів (Claessens 2014). Цікаво відзначити, що структура сімейства генів вар присутній з до П. триденної і П. reichenowi дивергенції, яке відбулося більше двох мільйонів років тому (Zilversmit 2013).
Ендотеліальні Рецептори клітин
Можливі Рецептори Виявлені
від In Vitro Binding Assays
CD36
Ig суперсімейства
ICAM1
VCAM-1
PECAM1
хондроитинсульфат
ендотеліального рецептора протеїну С
гепарансульфат
гіалуронова кислота
Е-селектину
тромбоспондин
Rosetting Ліганди
CR-1
групою крові Ag
глікозаміноглікани
Кілька можливих ендотеліальні рецептори (Box) були ідентифіковані шляхом тестування здатності інфікованих еритроцитів зв’язувати в статичних аналізах прилипання (Beeson and Brown 2002). Одна з кращих характеризується серед них є CD36, складовою мембранний білок 88 кДа, виявили на моноцитах, тромбоцитах і ендотеліальних клітинах. Заражені еритроцити від більшості паразитом ізолює зв’язуються з CD36 і зв’язує домен був зіставлений з CIDR з PfEMP1 (дивись малюнок). Проте, CD36 не було виявлено на ендотеліальних клітинах кровоносних судин головного мозку і паразитів з клінічних ізолятів, як правило, дотримуються обидві CD36 і внутрішньоклітинних молекул адгезії-1 (ICAM1). ICAM1 є членом надсемейства імуноглобулінів і функцій в міжклітинної адгезії. Крім того, уловлювання інфікованих еритроцитів і експресії ICAM1 було колокалізуются в головному мозку (Turner 1994).
Хондроітин сульфат A (CSA) було залучено в cytoadherence в плаценту і може сприяти негативний вплив P. малярійного під час вагітності. Роль деяких інших потенційних рецепторів не ясна. Наприклад, приєднання до тромбоспондин проявляє низьку афінність і не може підтримувати зв’язування в проточних умовах. Зв’язування з VCAM-1, PECAM1 і Е-selectin, як видається, рідкісні і питання про їх конститувною експресії на ендотеліальних клітинах були підвищені. Проте, cytoadherence може включати в себе кілька взаємодій рецептор / ліганд.
Rosetting ще один клейовий явище виставлені P. фальціпарум-інфікованих еритроцитів. Заражені еритроцити з деяких ізолятів паразита буде пов’язувати Многостержневим неінфікованих еритроцитів і PfEMP1 мабуть, грають певну роль, принаймні, якийсь rosetting. Можливі рецептори включають комплемент-рецептора-1 (CR1), групу крові антигену або глікозаміногліканових залишки на невстановленого протеогликана. (Дивіться малюнок із зображенням можливих взаємодій рецептор-ліганд, що беруть участь в rosetting на інший веб-сторінці.)
зв’язування фенотипів
домен рецептор
CIDR CD36
DBLa rosetting
DBLb ICAM-1,
DBLg CSA
Різні типи доменів двомісними і CIDR (описано вище), зв’язуються з різними рецепторами ендотеліальних клітин (Craig and Scherf 2001). Наприклад, DBLa, який включає перший домен, зв’язується з багатьма з рецепторів, асоційованих з rosetting. Зв’язування CIDR до CD36 може пояснити велику кількість цього специфічного зв’язування фенотипу серед паразитів ізолятів.
(Веб-сторінка зібрана Hagai Гінзбург містить докладні дані, що зображують багато аспектів господар-паразит взаємодії, в тому числі : Композиції регулятора і взаємодій рецептор-ліганд , PfEMP-1 структурою і специфічністю зв’язування , рецепторами ендотеліальних клітин і rosetting. Sherman et al (2003) розглянуті механізми cytoadherence.)
Антигенна мінливість
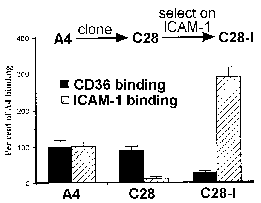
Робертс і ін 1992The кодування cytoadherence лиганда вельми поліморфного сімейства генів являє собою парадокс в тому receptor/ligand, як правило, вважається дуже специфічні. Цікаво відзначити, що вибір для різних cytoadherent фенотипів призводить до сопровождающемуся зміною типу поверхні антигенної (Biggs 1992). Аналогічним чином, дослідження клонових ліній паразитів показало, що зміни в типі поверхні антигенної корелюють з відмінностями в зв’язуванні з CD36 і ICAM1. Наприклад, батьківський лінія (А4) дотримувалася однаково добре до CD36 і ICAM1, в той час як один з А4, отриманих клонів (С28) виявляв явну перевагу CD36 (рис, змінену від Roberts 1992). Зв’язування з ICAM1 потім був обраний повторно панорамування заражених еритроцитів на ICAM1. Всі три паразита-клони (A4, С28, С28-I) виставлені різні антигенні типи як показали аглютинації з гіпер-імунних сироваток.
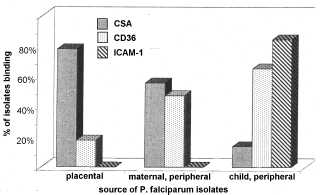
Вираз конкретного PfEMP1 призведе до паразита з яскраво вираженою cytoadherent фенотипу, і це також може впливати на патогенез і хвороби результат. Наприклад, зв’язування з ICAM-1, як правило, беруть участь в мозкової патології. Таким чином, паразити, які виражають PfEMP1, який зв’язується з ICAM1 може бути з більшою ймовірністю викликає церебральної малярії. Насправді, більш високі рівні транскрипції певних генів УАГ зустрічаються у випадках важкої малярії в порівнянні з неускладненій малярії (Rottmann 2006). Аналогічним чином, більш висока частка ізолятів, які зв’язуються з CSA отримують з плаценти в порівнянні з периферичному кровотоці або вагітних жінок або дітей (рис, модифікованому з Beeson 1999). Крім того, плацентарної малярії часто асоціюється з більш високим рівнем транскрипції певного гена вар, який пов’язує CSA (Duffy 2006). Це явище не обмежується плаценту в тому, що існує домінуючий вираз певних генів УАГ в різних тканинах (рис, з Montgomery 2007). Наступні роботи підтвердили, що різні варіанти PfEMP1 мають різні тропизмами для різних тканин (Smith 2014 року).
CSA Binding
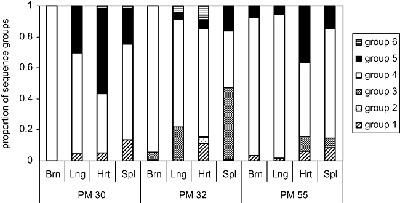
Малюнок, редагували Бісон тисяча дев’ятсот дев’яносто дев’ять Показує пропорції ізолятів, які зв’язуються з CSA, CD36 або ICAM-1. Заражені еритроцити були зібрані з плаценти, периферичного кровообігу матері, або периферичного кровообігу дитини. Малюнок, з Монтгомері 2007 показує співвідношення різних типів PfEMP1 (позначені як групи 1-6), виражені в різних тканинах (мозок, легені, серце і селезінка) від 3-х різних пацієнтів. PM30 помер від важкої малярійній анемії. PM32 був поставлений діагноз як церебральної малярії і важкої анемії. PM55 був діагностований тільки з церебральної малярії.
Зовсім недавно було показано, що виразний підмножина генів УАГ високо розшифровані наступний вибір на клітини мозку людини ендотеліальних і що ті ж самі різні підтипи пов’язані з церебральної малярії (Aird 2014; Cunnington 2013; Smith 2013). Ця тканина специфічна експресія певних генів УАГ увазі, що різні тканини вибору з різних паразитів популяцій на основі конкретного PfEMP1 експресуватися на поверхні інфікованої еритроцита.
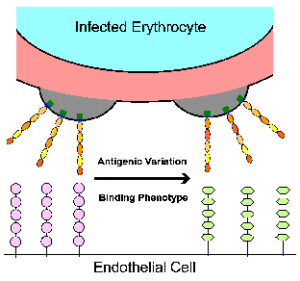
Незважаючи на те, секвестрації пропонує багато переваг для паразита, експресію антигенів на поверхні інфікованої еритроциті забезпечує мішенню для імунної системи господаря. Паразит лічильники імунної відповіді хазяїна шляхом експресії антигенно різних молекул PfEMP1 на поверхні еритроцита. Це дозволяє паразита уникнути зазору імунної системи господаря, але при цьому зберегти cytoadherent фенотип. Цей антигенний перемикання може відбуватися так часто, як 2% за покоління за відсутності імунного тиску (Roberts 1992). Молекулярний механізм антигенної перемикання не відомо. Експериментальні дані свідчать про те, що механізм не пов’язаний з дублюючими транспозиції в специфічні сайти експресії, пов’язані як знайти в Aфриканських трипаносом. Тільки один ген вар виражається в той час (тобто аллельного виключення). Чи не пов’язані експресується гени промовчали білками, які зв’язуються з областю промотора. Ген може активуватися перестановкою в певне місце в ядрі і пов’язана з хроматину модифікацією. Цей вислів пляма може вмістити тільки один активний промотор гена. Таким чином, промотор вар досить для обох глушників і моно-алельних транскрипції PfEMP1 алелі (Voss 2006; Guizetti 2013).
Резюме
Антигенна мінливість
Малярійний паразит змінює еритроцита шляхом експорту білків в клітку-господаря.
Одним з таких модифікацій є виразом PfEMP1 на поверхні еритроцита, який функціонує в якості ліганда cytoadherent.
Зв’язування цього ліганда з рецепторами на ендотеліальних клітинах-господарях сприяє секвестрації і дозволяє заражене еритроцит, щоб уникнути селезінку.
Численні гени PfEMP1 (тобто вар сімейство генів) забезпечують паразита за допомогою варіювати антиген, експресуватися на поверхні еритроцита.
Ця антигенної варіації також корелює з різними cytoadherent фенотипів.
Список використаної літератури
Адамс JH, Sim BKL, Долан С.А., Fang XD, Kaslow DC, Miller LH (1992) Сімейство еритроцита зв’язуючих білків паразитів малярії. Proc Natl Acad Sci USA 89, 7085-7089.
Ейрд WC, Mosnier LO Ферхерст RM (2014 року) малярійного плазмодія кирки (на) EPCR. Blood 123, 163-167.
Банністер LH, Мітчелл GH, М’ясник Г.А., Dennis ED, Cohen S (1986) Будова і розвиток поверхневого шару еритроцитарних мерозоїтів Plasmodium knowlesi. Cell Tissue Res 245, 281-290.
Бараль JC, Blisnick T, Фудзіока H, Alzari PM, Айкава M, Braun-Бретон C, Langsley G (1999) малярійного плазмодія субтілізін-протеази, як 2, а мерозоитов кандидат на мерозоитов поверхневого білка 1-42 maturase. Proc Natl Acad Sci U S A 96, 6445-6450.
Beeson JG, Brown GV (2002) Патогенез Plasmodium триденної малярії: роль адгезії паразита і антигенної мінливості. Cell. Mol. Life Sci. 59, 258-271.
Beeson JG, Brown Г.В., Моліна ME, Mhango C, Dzinjalamala F, Роджерсон SJ (1999) малярійного плазмодія ізолює від інфікованих вагітних жінок і дітей пов’язані з особливими липких і антигенні властивості. J Infect Dis 180, 464-472.
Besteiro S, Dubremetz JF, Лебрен M (2011) Рухомий вузол апікомплексні паразитів: ключова структура для вторгнення. Cell Microbiol 13, 797-805.
Біггс Б.А., Андерс РФ, Діллон HE, Davern KM, Martin M, Петерсен C, Brown GV (1992) Адгезія інфікованих еритроцитів венулярного ендотелій вибирає для антигенних варіантів малярійного плазмодія. J Immunol 149, 2047-2054.
Blackman MJ, Фудзіока H, Стаффорд WL, Саджида M, Клаф B, Флек SL, Айкава M, Грейнджер M, Hackett F (1998) A субтілізін-подібного білка в секреторних органелах малярійного плазмодія мерозоитов. J Biol Chem 273, 23398-23409.
Бойл MJ, Лангер C, Chan JA, Ходдер А.Н., Coppel RL, Андерс РФ, Beeson JG (2014 року) Послідовна обробка поверхневих білків мерозоїтів під час і після вторгнення в еритроцитах по малярійного плазмодія. Заражайте Імун 82, 924-936.
Braun-Бретон C, Перейра да Сілва LH (1993) протеаз Малярія і вторгнення червоних кров’яних клітин. Parasitol Сьогодні 9, 92-96.
Каррузерс В.Б., Сіблі LD (1997) Послідовна секреції білка з трьох різних органел токсоплазма супроводжує вторгнення фібробластів людини. Eur J Cell Biol 73, 114-123.
Классенс A, Гамільтон WL, Kekre M, Отто TD, Faizullabhoy A, Рейнер JC і Квятковський D (2014 року) Генерація антигенного різноманітності в малярійного плазмодія структурованим перегрупування генів Var під час мітозу. PLoS Genetics 10(12):e1004812..
Купер JA (1993) мерозоитов поверхневий антиген-1 Plasmodium. Parasitol Сьогодні 9, 50-54.
Скотопромисловців А.Ф., Berry D, J Баум (2012) Клітинна і молекулярна основа для малярійного паразита вторгнення людини червоних кров’яних тілець. J Cell Biol 198, 961,971.
Креб BS, Cooke BM, Рідер JC, Waller РФ, Каруана SR, Davern KM, Вікхем ME, Brown Г.В., Coppel RL, скотопромисловців AF (1997) Цілеспрямоване руйнування гена показує, що регулятори дозволяють малярії інфіковані червоні клітини cytoadhere при фізіологічному напруженні зсуву , Cell 89, 287-296.
Craig A, Scherf A (2001) Молекули на поверхні малярійного плазмодія інфікованих еритроцитів і їх роль в патогенезі малярії та імунної ухилення. Mol. Biochem. Parasitol. 115, 129-143.
Crosnier C, Бустаманте LY, Bartholdson SJ і ін (2011) Basingin є рецептором істотним для вторгнення в еритроцитах по малярійного плазмодія. Nature 480, 534-537.
Каннингтон AJ, Райлі EM Walther M (2013) Stuch в колії? Переглядаючи роль паразита секвестру в важких синдромів малярії. Tr Parasitol 29, 585-592.
Deitsch KW, дель Pinal A, Wellems TE (1999) внутрікластерних рекомбінації і вар транскрипційні перемикачі в антигенної мінливості малярійного плазмодія. Mol Biochem Parasitol 101, 107-116.
Deitsch KW, Wellems TE (1996) Мембранні зміни в еритроцитах паразитує малярійного плазмодія. Mol Biochem Parasitol 76, 1-10.
Даффі MF, Caragounis A, Noviyanti R, Kyriacou HM, Choong Е.К., Boysen К, цілитель J, Роу JA, Моліна ME, Brown Г.В., Роджерсон SJ (2006) транскрибується гени вар, пов’язані з плацентарної малярії в малавійських жінок. Infect. Immun. 74: 4875-4883.
Гоел В.К., Лі X, Лю SC, Чішті AH, Oh SS (2003) Band 3 є господарем зв’язування рецептора мерозоитов поверхневий білок 1 під час малярійного плазмодія вторгнення еритроцитів. Proc Natl Acad Sci 100, 5164-5169.
Gratzer WB, Dluzewski AR (1993) еритроцита і малярійного паразита вторгнення. Сьомін Hematol 30, 232-247.
Guizetti J, Scherf A (2013) Silence, активувати, врівноваженість і перемикач! Механізми антигенної мінливості малярійного плазмодія. Cell Microbiol 15, 716-726.
Хан Ю.С., Томпсон J, Kafatos FC, Барільяс-Мури C (2000) молекулярних взаємодій між клітинами середньої кишки Anopheles stephensi і Plasmodium berghei: час теорії бомби ookinete нашестя комарів. EMBO J 19, 6030-6040.
Тримач AA, Blackman MJ, Борре M, Burghaus PA, Чаппел JA, Keen JK, Лінг IT, Огун SA, Оуен CA, Сінха К.А. (1994) малярійних паразитів в еритроцитах вторгнення. Biochem Soc Транс 22, 291-295.
Hviid L, Йенсен ATR (2015) PfEMP1 Тау паразит сімейства білків, що мають ключове значення в імунітеті Plasmodium триденної малярії і патогенез. Advances in Parasitology 88, 51-84.
Kappe SHI, Buscaglia CA, Бергман LW, Коппенс I, Nussenzweig V (2004) апікомплексні ковзаючи моторики і інвазія клітина-господар: капітального ремонту моделі двигуна. Trends in Parasitology 20, 13-16.
Leykauf K, Treeck M, Gilson PR, NEBL T, Braulke T, скотопромисловців А.Ф., Gilberger TW, Креб BS (2010) протеїнкінази залежне фосфорилювання апикального мембранного антигену 1 планує важливу роль в еритроцитах інвазії малярійного паразита. PLOS Pathogens 6, e1000941.
Мітчелл GH, Томас AW, Margos G, Dluzewski AR, Банністер LH (2004) апікальної мембрани антиген 1, основним кандидатом вакцини проти малярії, є посередником тісний прихильність інвазивних мерозоїти для розміщення червоних кров’яних клітин. Infect. Імун. 72, 154-158.
Монтгомері J, Mphande FA, Berriman M, болі A, Роджерсон SJ, Taylor TE, Моліна ME, Craig генної експресії вар (2007) Диференціал в органах хворих, які помирають від триденної малярії. Molecular Microbiology 65, 959-967.
Мота М.М., Pradel G, Вандерберг GP, Hafalla JCR, Фреверт U, Nussenzweig RS, Nussenzweig V, Родрігеса A (2001) Міграція Plasmodium спорозоїтів через клітини до зараження. Наука 291, 141-144.
Про SS, Фойгт S, Fisher D, Yi SJ, Лерой PJ, Дерік LH, Лю SC, Чішті AH (2000) малярійного плазмодія в еритроцитах мембранний білок 1 прикріплюється до спектрінового-актину стик і ручку-асоційований багату гистидином білок еритроцит цитоскелета , Mol Biochem Parasitol 108, 237-247.
Рід MB, Каруана SR, Бачелор AH, Томпсон JK, Креб BS, скотопромисловців AF (2000) Цілеспрямоване руйнування зв’язує антигену еритроцитів в малярійного плазмодія, пов’язаний з переходом у напрямку до сиаловой кислоті незалежного шляху вторгнення. Proc Natl Acad Sci USA 97, 7509-7514.
Робертс DJ, Craig AG, Берендт AR, Pinches R, G Неш, Marsh K, Newbold CI (1992) Швидке перемикання на кілька антигенних і клейових фенотипів при малярії. Природа 357, 689-692.
Rottmann M, Lavstsen T, Mugasa JP, Kaestli M, Jensen ATR, Мюллер D, Theander T, Бек HP (2006) Диференціальна експресія генів груп УАК пов’язана з захворюваністю, викликаної Plasmodium триденної інфекції в танзанійських дітей. Infect. Immun. 74, 3904-3911.
Sam-Yellowe TY (1996) Rhoptry органел Apicomplexa: їх роль в інвазії клітини-господаря і внутрішньоклітинного виживання. Parasitol Сьогодні 12, 308-316.
Сантос JM і Солдати-Фавр D (2011) фактори вторгнення пов’язані з ключовими сигнальних подій, що ведуть до створення інфекції в апікомплексні паразитів. Cellular Microbiology 13, 787-796.
Шерф A, Hernandez-Rivas R, стіл P, Bottius E, Benatar C, Pouvelle B, Гайсин J, Ланзер M (1998) Антигенна мінливість малярії: при перемиканні на місці, розслабленими і взаємовиключними транскрипції генів УАГ під час всередині еритроцитарного розвитку в малярійного плазмодія. EMBO J 17, 5418-5426.
Шарма P, Chitnis CE (2013) Ключові молекулярні події під час вторгнення клітини-господаря апікомплексні патогенів. Curr опіно Microbiol 16, 432-437.
Шерман IW, Крандалл IE, Гатрі N, Land KM (1995) Липкі секрети секвестру. Parasitol Сьогодні 11, 378-384.
Шерман IW, Еда S, Винограду E (2003) Cytoadherence і секвестрації малярійного плазмодія: визначення зв’язків, які пов’язують. Мікроби і інфекції 5, 897-909.
Sinnis P, Sim BKL (1997) Cell вторгнення хребетних етапів Plasmodium. Tr Microbiol 5, 52-58.
Сміт JD (2014 року) Роль PfEMP1 класифікації області адгезії в Plasmodium досліджень фальціпарум патогенезу. Mol Biochem Parasitol 195, 82-87.
Сміт JD, Роу JA, Хіггінс MK Lavstsen T (2013) смертельної захоплення малярію: cytoadhesion з малярійного плазмодія-інфікованих еритроцитів. Cell Microbiol 15, 1976-1983.
Тем WH, Цілитель J, скотопромисловців AF (2012) еритроцита і ретикулоцитів зв’язування подібні білки малярійного плазмодія.Tr Parasitol 28, 23-30.
Tomley FM, Сольдаті DS (2001) Модулі Комбінуйте: структура та функції білків microneme в апікомплексні паразитів. Тенденції Parasitol. 17, 81-88.
Тонкін ML, Рокес M, Ламарк MH, Pugniere M, ┬аDouguet D, J Кроуфорд, Лебрен M, Буланже MJ (2011) клітина-господар Вторгнення апікомплексні Паразити: Insights від співпраці Структура AMA1 з Ron2 пептидом. Science 333, 463-467.
Turner GDH, Моррісон H, Джонс М, Девіс TME, Looareesuwan S, Buley ID, Gatter KC, Ньюболд CI, Pukritayakamee S, Nagachinta B, білий NJ, Берендт AR (1994) Імуногістохімічне дослідження патології зі смертельними наслідками малярії – свідоцтво широко поширеною активації ендотелію і потенційна роль міжклітинної адгезії-1 в корі головного секвестру. Am J Pathol 145, 1057-1069.
Восс TS, Цілитель J, Marty AJ, Даффі MF, Томпсон JK, Beeson JG, Рідер JC, Креб BS, скотопромисловців AF (2006) вар ген контролює промотор аллельного виключення генів вірулентності в Plasmodium триденної малярії. Nature 439: 1004-1008.
Уоллер KL, Cooke BM, Nunomura W, Мохандас N, Coppel RL (1999) Відображення зв’язують доменів, що беруть участь у взаємодії між малярійного плазмодія ручкою-асоційованої гистидин багатих білком (KAHRP) і cytoadherence лиганда P. фальціпарум мембран еритроцитів Protein- 1 (PfEMP1). J Biol Chem 274, 23808-23813.
Waterkeyn JG, Вікхем ME, Davern KM, Cooke BM, Coppel RL, Рідер JC, Culvenor JG, Waller РФ, скотопромисловців А.Ф. (2000) спрямований мутагенез малярійного плазмодія еритроцита мембранного білка 3 (PfEMP3) порушує cytoadherence малярії інфікованих червоних кров’яних клітин , EMBO J 19, 2813-2823.
Zieler H, Dvorak JA (2000) Вторгнення в пробірці з клітин комарів середньої кишки за рахунок доходів паразита малярії за консервативним механізмом і призводить до загибелі клітин інвазованих середньої кишки. Proc Natl Acad Sci 97, 11516-11521.
Zilversmit М.М., Чейз Е.К., Чень DS, Awadalla P, день КП і McVean G (2013) гіперваріабельний гени антигену малярії мають давнє коріння. BMC Evolutionary Biology 13:110.
Zuccala ES і Baum J (2011) цитоскелету і мембрани ремоделювання під час малярійного паразита вторгнення людини eythrocyte. British J Haematology 154, 680-689.
ПОСИЛАННЯ
Toп
Хост Вторгнення еритроцитів
Хост Модифікація еритроцитів
Посилання
Біохімія
Малярія Примітки Клас
Глосарій
Інші лекції та викладання
Уайзер Головна сторінка