Original: http://chemed.chem.purdue.edu/genchem/topicreview/bp/ch18/soluble.php
Чому певні тверді тіла розчиняються у воді?
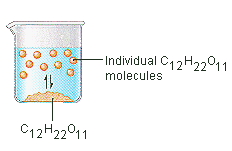
Він бере енергію, щоб розірвати зв’язки між молекулами C12H22O11 сахарози. Він також приймає енергію, щоб розірвати водневі зв’язку в воді, які повинні бути зруйновані, щоб вставити один з цих молекул сахарози в розчин. Цукор розчиняється в воді, оскільки енергія виділяється, коли злегка полярні молекули сахарози утворюють міжмолекулярні зв’язки з полярними молекулами води. Слабкі зв’язку, які утворюють між розчиненим речовиною і розчинником компенсацією енергії, необхідної, щоб зруйнувати структуру як в чистому розчиненому речовині і розчинник. У разі цукру і води, цей процес працює так добре, що до 1800 р. сахарози може розчинити в літрі води.
Іонні тверді речовини (або сіль) містять позитивні і негативні іони, які утримуються разом за рахунком сильної сили тяжіння між частинками з протилежними зарядами. Коли один з цих твердих речовин розчиняються у воді, іони, які утворюють тверді вивільняються в розчин, де вони стали асоціюватися з полярними молекулами розчинника.

| H2O | ||||
| NaCl(s) | Na+(aq) | + | Cl–(aq) |
В цілому можна вважати, що солі розкладаються на іони, коли вони розчиняються у воді. Іонні сполуки розчиняються у воді, якщо енергія виділяється, коли іони взаємодіють з молекулами води компенсує енергію, необхідної, щоб розірвати іонні зв’язку в твердому і енергії, необхідної для поділу молекул води, так що іони можуть бути вставлені в розчин.
Обговорення розчинності рівноваг засновані на наступному допущенні: коли тверді речовини розчиняються у воді, вони дисоціюються на елементарні частинки, з яких вони утворені. Таким чином, молекулярні тверді частинки диссоциируют з отриманням окремих молекул
| H2O | ||
| C12H22O11(s) | C12H22O11(aq) |
а іонні тверді частинки диссоциируют з отриманням розчинів позитивних і негативних іонів, які вони містять.
H2O
| NaCl(s) | Na+(aq) | + | Cl–(aq) |
Коли сіль спочатку додають, вона розчиняється і швидко дисоціює. Провідність розчину, отже, швидко збільшується в першу чергу.
розчинення
| NaCl(s) | Na+(aq) | + | Cl–(aq) |
розмежування

Концентрації цих іонів незабаром стануть досить великими, що зворотна реакція починає конкурувати з прямою реакцією, що призводить до зменшення швидкості, з якою іони Na+ і Cl– увійти в розчин.
сполучення
| Na+(aq) | + | Cl–(aq) | NaCl(s) |
осідання
У кінцевому рахунку Cl– концентрації іонів Na+, і стати досить великими, що швидкість, при якій відбувається осадження точно врівноважує швидкість, з якою розчиняється NaCl. Як тільки це відбудеться, немає ніяких змін в концентрації цих іонів з плином часу і реакція знаходиться в рівновазі. Коли ця система досягає рівноваги його називають насиченим розчином, так як він містить максимальну концентрацію іонів, які можуть існувати в рівновазі з твердою сіллю. Кількість солі, яке повинно бути додано в заданому обсязі розчинника з утворенням насиченого розчину називається розчинність солі.
Є цілий ряд закономірностей в даних, отриманих в результаті оцінки розчинності різних солей. Ці моделі формують основу для правил, викладених у наведеній нижче таблиці, які можуть визначати напрямок передбачення буде дана сіль розчиняється у воді. Ці правила засновані на наступних визначень термінів розчинних, нерозчинних і малорозчинних.
• Сіль розчиняється, якщо вона розчиняється в воді з отриманням розчину з концентрацією щонайменше, 0,1 моля на літр при кімнатній температурі.
• Сіль є нерозчинним, якщо концентрація водного розчину складає менше 0,001 М при кімнатній температурі.
• Злегка розчинні солі дають рішення, які потрапляють між цими двома крайностями.
Правила розчинності для іонних сполук у воді
|
Розчинні солі |
| 1. Іони Na+, K+ і NH4+ утворюють розчинні солі. Таким чином, NaCl, KNO3, (NH4)2SO4, Na2S і (NH4)2CO3 розчинні. |
| 2. Нітратний іон (NO3–) утворює розчинні солі. Таким чином, Cu(NO3)2 і Fe(NO3)3 розчинні. |
| 3. Іони хлориду (Cl–), броміду (Br–) та йодиду (I–) загалом формують розчинні солі. Винятками з цього правила є іони солей Pb2+, Hg22+, Ag+ і Cu+. ZnCl2 розчинний, а CuBr ні. |
| 4. Іон сульфату (SO42-) загалом формує розчинні солі. Винятками є нерозчинні BaSO4, SrSO4 і PbSO4, а Ag2SO4, CaSO4 і Hg2SO4 є малорозчинними. |
|
Нерозчинні солі |
| 1. Сульфіди (S2-) зазвичай нерозчинні. Винятками є Na2S, K2S, (NH4)2S, MgS, CaS, SrS і BaS. |
| 2. Оксиди (O2-) зазвичай нерозчинні. Винятками є розчинні Na2O, K2O, SrO і BaO, а CaO є малорозчинним. |
| 3. Гідроксиди (OH–) зазвичай нерозчинні. Винятками є розчинні NaOH, KOH, Sr(OH)2 і Ba(OH)2, а Ca(OH)2 є малорозчинним. |
| 4. Хромати (CrO42-) зазвичай нерозчинні. Винятками є Na2CrO4, K2CrO4, (NH4)2CrO4 і MgCrO4. |
| 5. Фосфати (PO43-) і карбонати (CO32-) зазвичай нерозчинні. Винятками є іони солей Na+, K+ і NH4+. |
